Enfoque práctico para manejo de dermatitis atópica por pediatras y generalistas.Autor: Lawrence F. Eichenfield, MDa, Mark Boguniewicz, MDb, Eric L. Simpson, MDc, John J. Russell, MDd, Julie K. Block, BAe, Steven R. Feldman, MD, PhDf,g, Adele R. Clark, PA-Cf, Susan Tofte, BSN, MS, FNP-Ch Fuente: Pediatrics. 2015 Sep;136(3):554-65. doi: 10.1542/peds.2014-3678. Epub 2015 Aug 3.
Se estima que en 2009 -2011, la dermatitis atópica (DA) afectó al 12,5% de los niños (0-17 años de edad) en los Estados Unidos, con un aumento de poco más de 5% desde 1997 hasta 1999. 1Entre estos pacientes, la gran mayoría (~67%) presentaron 2enfermedad leve y como tal pudo ser manejada adecuadamente por el pediatra u otros prestadores de atención primaria (PAP)/ médico de cabecera. Sin embargo, la mayoría de los pediatras derivan incluso a sus pacientes con patología leve a los dermatólogos (~ 85%) y proporcionan una atención inicial única y limitada (81%).
Sean o no pacientes derivados a dermatología3, pediatras y médicos de familia seguirán desempeñando un papel central en el manejo para un seguimiento regular, el tratamiento de mantenimiento, la educación continua en pacientes internados y cuidadores, y el contacto de primera línea para los brotes y las complicaciones, como la infección estafilocócica secundaria.
El 6 de septiembre de 2013, se convocó una mesa redonda para discutir los retos en el manejo de la DA junto con las oportunidades de mejorarla a través de una variedad de disciplinas. Esta mesa redonda fue la única que incluyó un paciente abogado, así como representantes de la dermatología (general y pediátrica), alergia-inmunología pediátrica, medicina familiar, cuidado administrado, y de enfermería. Durante el debate, se hizo evidente que las guías de manejo de la DA actuales carecen de ciertos elementos que pueden mejorar su utilidad práctica, especialmente para los prestadores de atención primaria incluyendo los pediatras.
Este artículo evaluará:
(1) la utilidad de las guías actuales,
(2) presentará un modelo de tratamiento integrado, específico para médicos de cabecera, basado en las guías actuales y la evidencia clínica,
(3) dará consejos prácticos sobre la aplicación y optimización de los escritos, los planes de tratamiento individualizados para los pacientes, y
(4) proporcionará recomendaciones para mejorar la utilidad de las futuras guías, todas ellas basadas en los trabajos de la reunión.
Abreviaturas:
AAAAI: Academia Americana de Alergia, Asma e Inmunología
AAD: Academia Americana de Dermatología
ACAAI: Colegio Americano de Alergia, Asma e Inmunología
AD: atópica dermatitis
EDF: Foro Europeo de Dermatología
FTU: unidad de la punta del dedo
HCP: cuidado de la salud
NEA: Asociación Nacional de Eczema
PCP: proveedor de atención primaria
TCI: inhibidor tópico de la calcineurina
WWT: la terapia de abrigo mojado
Guía de manejo reciente en dermatitis atópica:
Para mejorar la utilidad, las guías de manejo deben contener un algoritmo de tratamiento conciso basado en la severidad,que no sea rígido (es decir, permitir situaciones de pacientes únicos) con instrucciones para cuando se da un paso hacia arriba o hacia abajo en el tratamiento. La evaluación de criterios de diagnóstico y la gravedad se deben incluir para proporcionar un marco para la evaluación inicial y permanente. Además, las guías deben reflejar la entrada multidisciplinaria y ser libre y fácilmente accesible a todos los proveedores de atención de salud (PAS), independientemente de su especialidad.
Con cada iteración, las guías de manejo de DA han mejorado según los fundamentos de American Academy of Dermatology’s (AAD) Guidelines4 2004 and American College of Allergy, Asthma, y Immunology (ACAAI)/American Academy of Allergy, Asthma, and Immunology’s (AAAAI) Practice Parameters5 through the 2006 European Academy of Allergology y Clinical Immunology (EAACI)/AAAAI Guidelines6 to the current 2012 European Dermatology Forum (EDF) Guidelines,7,8 2012 AAAAI/ACAAI Practice Parameter Update (published in 2013),9 and 2014 AAD Guidelines10–13. De particular interés, las 2012 AAAAI/ACAAI Practice Parameter and EDF Guide lines incluyen los aportes de los profesionales sanitarios, tanto de alergia / inmunología y dermatología y especifican que sus recomendaciones pueden ser útiles para los profesionales sanitarios fuera de esas áreas terapéuticas. Las Directrices del FED 2012 son únicos en la prestación de recomendaciones para las cantidades mensuales de los corticosteroides tópicos para prescribir y la forma de cuantificar las cantidades diarias de fármaco tópico para los pacientes.
Integración de Guías con evidencia clínica
Con tantas guías de manejo de DA promulgadas por diferentes grupos, existe la posibilidad de que éstos entren en conflicto entre sí, por lo que es difícil para los profesionales de la Salud determinar cuáles son las pautas más adecuadas para sus pacientes. El consenso entre los participantes de la mesa fue que los PAP (médicos de cabecera) podrían beneficiarse con un plan de sistema integrado más sencillo y específico, que se acomode a la mayoría de los casos encontrados, y proporcione orientación sobre cuándo derivar a un dermatólogo o alergólogo / inmunólogo.
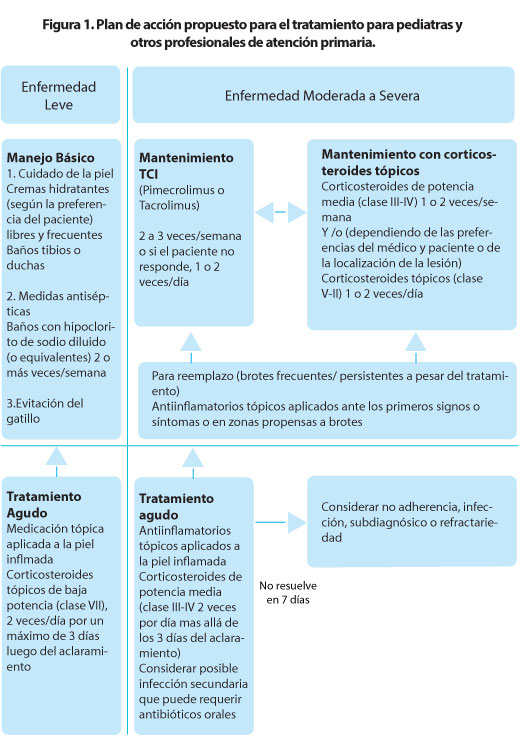
Además, algunas guías contienen un modelo de tratamiento y, aquellos que lo tienen, no logran dar cuenta de la naturaleza de la recaída-remisión de la DA o para el uso del proactivo. Para hacer frente a estas deficiencias y proporcionar una herramienta útil para los pediatras y los médicos de cabecera en el manejo de sus pacientes con DA, los autores proponen el siguiente modelo de diagnóstico y tratamiento basado en las Guías EDF 2012,7,8 de Parámetros y Práctica de la ACAAI y AAAAI 2012,9 y Guías de la AAD 2014 10-13 publicadas con evidencia clínica como apoyo. (Figura 1)
Haciendo el Diagnóstico
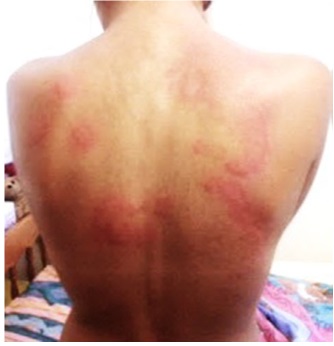
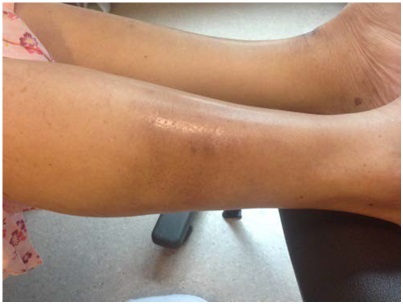
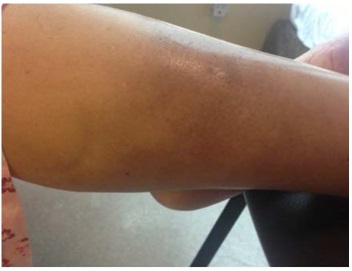
Debido a que no existe una prueba de laboratorio definitiva, el diagnóstico de esta enfermedad se hace en base a una combinación de síntomas clínicos: dermatitis pruriginosa que es crónica y / o recidivante con una distribución característica (cara, cuello, y superficies de extensión en los lactantes y los niños; pliegues de flexión en pacientes de cualquier edad).
El diagnóstico se realiza a menudo durante una exacerbación aguda de la inflamación de la piel que se caracteriza por prurito intenso, pápulas eritematosas y parches acompañados de piel seca (es decir, xerosis), excoriaciones y exudado, a veces, seroso.
Los criterios diagnósticos que figuran en las Guías AAD14 proporcionan un conjunto de criterios fáciles de usar que reflejan muchos criterios más largos validados. Un diagnóstico de DA solo debe ser hecho cuando se han descartadootras condiciones como la dermatitis irritante de contacto, psoriasis, sarna, o un exantema viral.
Se han propuesto una variedad de sistemas de puntuación para cuantificar la gravedad de la DA.
La enfermedad leve generalmente implica menos área de superficie del cuerpo, tiene un curso mas remitido y por supuesto se asocia con una menor intensidad prurito.15 Los pacientes que pueden ser mantenidos con el cuidado básico la mayoría de las veces tienen enfermedad leve.
Los pacientes con enfermedad moderada a severa pueden tener mayor participación de superficie corporal con un curso más continuo y prurito mas intenso.15 Estos pacientes a menudo requieren más la terapia de mantenimiento.
Manejo Básico
Independientemente de la gravedad de la enfermedad, las estrategias básicas de manejo deben ser implementadas para cada paciente diagnosticado con DA. Estas deben incluir el cuidado apropiado de la piel (es decir, la hidratación y humectación aplicadas a toda la piel), medidas antisépticas (es decir, baños de lavandina diluida), y la evitación del disparador (evitar irritantes en general como se identifica para cada paciente), con tratamiento agudo añadido según sea necesario para brotes (es decir, intensificación aguda de los síntomas y la inflamación de la piel necesitando una escalada en el tratamiento y / o consejo médico16).
Tratamiento de los brotes agudos
Dependiendo del paciente y de la preferencia del médico, el tratamiento de brotes agudos puede ser controlado con un corticosteroide tópicos de diversa potencia,17 y los corticoides tópicos de mediana potencia (por ejemplo, Clase III-IV) se utilizan a menudo durante varios días a unas pocas semanas.11 La terapia subsiguiente de mantenimiento depende entonces de la gravedad, así como de la persistencia de los signos y síntomas de DA.
Terapia de mantenimiento para la enfermedad leve
Después de que el brote inicial ha sido controlado, muchos pacientes con DA leve o más episódica podrán mantener el control de la enfermedad con tratamiento básico con: hidratantes, cuidado de la piel, etc., regresando intermitentemente al tratamiento agudo con corticosteroides tópicos cuando sea necesario para los brotes. El uso de humectantes solos como terapia de mantenimiento, sin antiinflamatorios tópicos, suele ser suficiente para la DA leve. Los pacientes cuyos síntomas no están bien controlados con tratamiento básico se considera que tienen enfermedad moderada a severa.
Terapia de mantenimiento para enfermedad moderada a severa
Los pacientes con DA de moderada a severa pueden requerir terapia de mantenimiento "proactivo" aplicada regularmente a la piel de aparencia normal en las zonas propensas a brotes y / o aplicada ante los primeros signos o síntomas de un brote con tacrolimus o pimecrolimus (inhibidores tópicos de la calcineurina [TCI]) o corticosteroides tópicos de mediana potencia (por ejemplo, Clase III-IV, a excepción de la cara y ojos).
Tacrolimus 18-21 y fluticasona 22 han sido estudiados en ensayos clínicos a largo plazo de 2 a 3 veces de aplicación semanal. Alternativamente, un paciente puede recibir una a dos veces al día TCI (pimecrolimus o tacrolimus); también se han realizado pruebas clínicas en este escenario.23,24 Aunque no han sido estudiados los corticoides de baja potencia tópica (Clase V-VII), aplicados localmente una a dos veces al día en zonas propensas a la recurrencia, son utilizados por muchos pacientes para mantener el control de la enfermedad.
La elección de TCI versus corticosteroides tópicos para terapia de mantenimiento depende del paciente/cuidador y de la preferencia del proveedor, el acceso a los medicamentos (incluyendo formulario de estado y costo de los medicamentos), la localización de la lesión (el uso de corticosteroides tópicos en zonas de piel sensible tales como la cara y los ojos debe ser limitado), y la efectividad y tolerancia observada con un agente particular.
Además, para el uso a largo plazo, es importante utilizar la potencia más baja del corticosteroide tópico que sea eficaz para minimizar el riesgo de efectos adversos (atrofia cutánea, telangiectasias, estrías, glaucoma, brote rebote, adicción / retiro a los corticosteroides tópicos, taquifilaxia, enfermedad de Cushing, supresión adrenocortical, disminución del crecimiento) 25; esto es particularmente cierto para sitios de piel sensible, tales como la cara, el cuello, y "área del pañal." 11 La falta de adecuada supresión de la inflamación de la piel no sólo perpetúa el malestar sino que induce también al rascado continuo y a un mayor riesgo de infección.
Optimizar e Individualizar
Planes de Tratamiento
Cuando se diseña un plan de tratamiento para un paciente específico, el médico debe basarse en la edad del paciente, los fracasos de tratamientos anteriores, a quien va destinada la prestación de la atención (niños / bebés), localización de la lesión (el uso del corticosteroide tópico debe ser limitado en potencia y duración de la aplicación para áreas sensibles de la piel), el seguro del paciente y los recursos financieros para obtener medicamentos, estilo de vida familiar (es decir, el tiempo para los baños y la aplicación de crema hidratante y crema antiinflamatoria tópica), y las preferencias del paciente (buscar la sensación de ungüentos frente a cremas). Las preferencias del paciente / cuidador son especialmente importantes cuando se selecciona una formulación humectante porque la xerosis es la característica central de la DA.
Las lociones que contienen conservantes, fragancias, y otros productos químicos, pueden causar reacción alérgica o reacciones irritantes. Las lociones tienen un alto contenido de agua y, especialmente en los pacientes más gravemente xeróticos, pueden producir sequedad; por lo que pueden ser preferibles los ungüentos humectantes con mayor contenido de aceite y sin conservantes.9,11 La elección de la crema hidratante debe basarse en la preferencia / tolerancia del paciente para la oclusividad de pomadas o aceites frente a la crema.
Deben tenerse en cuenta consideraciones similares ante las preferencias para la formulación de tópicos antiinflamatorios, así como consideración por el costo de la medicación. Se debe notar que diferentes formulaciones de los mismos corticosteroides tópicos, incluso la misma concentración, pueden tener diferentes potencias, por ejemplo la pomada de furoato de mometasona 0,1% es de alta potencia (clase II), mientras que el furoato de mometasona 0,1% crema es de potencia media (clase III-IV).
La determinación específica de los desencadenantes de la DA del paciente es un reto, pero si éstos factores pueden ser identificados, la evitación puede dar lugar a intervalos más largos entre brotes e incluso el aclaramiento completo de la enfermedad en algunos casos. Los desencadenantes inespecíficos pueden incluir jabones fuertes, detergentes, lana, y otros tejidos abrasivos, ropa ajustada, ciertos productos químicos (por ejemplo, formaldehído utilizado para dimensionamiento de tela), irritantes en el aire (el humo del tabaco, la contaminación del aire), y / o transiciones en los extremos de temperatura y humedad.
En raras ocasiones, las alergias pueden ser desencadenantes de la dermatitis, y las alergias ambientales y alimentarias son más comunes en los niños con DA que en los que no la tienen.13 La sensibilización para la alimentación y los alérgenos ambientales pueden ser identificados mediante punción cutánea o pruebas de IgE específicas, y la alergia de contacto puede ser evaluada a través de parches de prueba.
Sin embargo, los proveedores de salud no deben sugerir pruebas de rutina para buscar "causas" de DA, ya que el valor predictivo de las pruebas positivas es bajo y, a menudo verdaderas alergias clínicas pueden ser irrelevantes como desencadenantes de DA (por ejemplo, puede causar una reacción, tal como urticaria o picazón, sin que necesariamente se produzca un brote de DA) 9,13
Los alérgenos "relevantes" difieren por grupos de edad: los niños pequeños son más propensos a tener alergia a los alimentos (aunque la minoría de lactantes y niños que muestran reactividad a través pinchazo o análisis de sangre tienen alergia clínica cierta), mientras que niños mayores y adultos son más propensos a tener sensibilidad a aeroalergenos.9,13 Muchos pacientes experimentan perturbación del sueño, especialmente durante los brotes, que afecta no sólo negativamente la calidad de vida, sino también puede aumentar el riesgo de hiperactividad-impulsividad y otros trastornos de la salud mental.
Se han reportado asociaciones positivas entre DA y desorden de hiperactividad por déficit de atención, 26-30 trastornos de ansiedad, 26,30 y depresión, 30 y trastornos del espectro autista30, especialmente entre los pacientes con DA y pérdida de sueño.28-30 En los pacientes que tienen una importante demanda de pérdida de sueño o que tienen factores de riesgo de 1 o más de estas comorbilidades de salud mental, pueden beneficiarse con antihistamínicos (hidroxizina o doxepina),31 antiinflamatorios tópicos,32–34 emolientes,35 hipnoterapia,36 y/o reducir los estímulos sensoriales puede ser beneficioso.
Finalmente, todos los planes de tratamiento deben incluir un seguimiento programado (llamada telefónica, consultorio, etc.), de manera óptima dentro de 1 a 2 semanas después de la visita inicial, para evaluar la adherencia al tratamiento y la satisfacción del paciente / cuidador y el nivel de confort con el plan. El seguimiento temprano puede conducir a una mejor adherencia y mejores resultados del tratamiento.
Implementación del plan de tratamiento de comunicación con los pacientes y cuidadores
Plan de Tratamiento Escrito
La incorporación de instrucciones en un plan escrito (similar a lo que es comúnmente implementado para pacientes con asma) con respecto a cuándoaplicar hidratantes y medicamentos tópicos, cuando dar un paso arriba o hacia abajo en el tratamiento, cuándo buscar consejo médico, evitar los desencadenantes, etc., es fundamental para garantizar una buena adherencia del tratamiento a largo plazo. La conversión actual de la historia clínica electrónica presenta una oportunidad para automatizar la creación de planes. Además, los folletos del plan de tratamiento son de libre disponibilidad para la duplicación y distribución a pacientes y/o cuidadores.38
Educación de paciente y cuidador
Es importante para los pacientes, cuidadores y miembros de la familia entender la naturaleza crónica de recaída-remisión de la DA y cómo implementar un plan escrito de tratamiento, incluyendo el cuidado adecuado de la piel, medidas antisépticas, evitación de disparadores, y tratamiento farmacológico, puede ayudar a extender los períodos de remisión. El proceso de educación del paciente / cuidador debe comenzar con el desarrollo inicial del plan y continuará a través de cada visita de seguimiento (especialmente cuando el plan de tratamiento se haya modificado) con el médico, enfermera u otro personal de salud, para asegurar que la corriente plan de tratamiento se entiende bien.
Además, el tiempo dedicado a la educación proporciona al médico (u otro prestador de salud) la oportunidad de corregir cualquier concepto erróneo que los pacientes y / o cuidadores puedan tener y abordar proactivamente frente a cualquier posible cuestión de seguros o de distribución de medicamentos, si fuera requerido.
Los pacientes / cuidadores deben recibir instrucciones sobre el cuidado apropiado de la piel, incluyendo hidratación de la piel con, baños o duchas de agua tibia, inmediatamente seguido de la aplicación de una cantidad adecuada de crema hidratante la piel húmeda.8,9,11
Además, la adición de una pequeña cantidad de lavandina (hipoclorito de sodio; ~ 0,5 tazas por 40 galones de agua (bañera llena) o 1 ml / l) dos veces por semana ha demostrado que reduce la severidad de la DA. El uso diario de estos baños con lavandina diluída o productos comparables en la ducha o el baño40 puede ser necesaria como parte de la terapia de mantenimiento de niños moderada a severamente afectados (aunque el efecto del manejo de la colonización bacteriana recurrente no ha sido establecida41).
La técnica se puede modificar para compresas locales o para el mantenimiento de las áreas que más a menudo muestran una infección secundaria o para pacientes con infección actual que no pueden tolerar el baño. El cuidado adecuado de la piel también ayudará a reducir la exposición y/o el impacto de ciertos factores desencadenantes de DA mediante el aumento del umbral para la irritación de la piel del paciente.
La Terapia Wet-wrap ((WWT envoltorio húmedo), con o sin corticoides tópicos podría reducir la gravedad de la enfermedad, especialmente para pacientes con DA moderada a severa durante los brotes11; sin embargo, la WWT puede llevar mucho tiempo y ser complicada. Los pacientes / cuidadores deben ser instruidos en la aplicación de vendajes tubulares, gasa, o ropa de algodón, suelta y humedecida (empapada en agua tibia, luego escurrida hasta que esté ligeramente húmeda) sobre corticosteroides tópicos o crema hidratante, seguida de una capa exterior seca de material similar (nunca envoltura de plástico), que puede ser usado por varias horas hasta 24 horas y repetida durante varios días por 2 semanas.42 Se debe tener cuidado durante la WWT, especialmente cuando se utiliza potencia media-alta de corticosteroides tópicos, debido al aumento de la penetración de la medicación y el riesgo de infección.
Se debe aconsejar a los pacientes / cuidadores evitar los irritantes inespecíficos mediante el uso de jabones suaves o productos de limpieza sin jabón, el uso de ropa "suave" / no irritante que es suelta y evitar el uso de suavizantes con fragancia para la ropa.9,13 Además, la exposición a los aeroalergenos (moho, ácaros del polvo, el polen, los animales caspa, irritantes en el aire), y extremos de temperatura y humedad se pueden evitar, o minimizar mediante el uso de aire acondicionado y / o filtros de aire.9 Los pacientes / cuidadores también deben ser instruidos sobre las estrategias de evitación de desencadenantes para DA específica para ellos (es decir, los alimentos, el contacto y los aeroalergenos) determinados a través del plan de optimización y la individualización.
También es de vital importancia instruir a los pacientes / cuidadores en la cantidad de medicación tópica y crema hidratante a usar en cada aplicación y la cantidad total a esperar que se consuma por semana o mes. La unidad de la punta del dedo (FTU - fingertip unit) se ha desarrollado como una herramienta útil para describir cuantitativamente a los pacientes / cuidadores la cantidad de medicación tópica para ser usada.44,45 Se define como la cantidad de ungüento expresada a partir de un tubo con un diámetro de 5 mm de boquilla medida desde el pliegue de la piel distal a la punta de la superficie palmar de un el dedo índice de adulto.
Esto es igual a ~ 0,5 g y es una cantidad adecuada "fina y uniforme" para la aplicación a un área de la piel igual a aproximadamente las 2 manos de un adulto con los dedos juntos. El número de FTUs requerido para el tratamiento de diferentes áreas del cuerpo varía con la edad del paciente, pero son FTUs medido con relación a manos de adultos / los dedos independientemente de la edad. Los médicos también pueden encontrar útil prescribir cantidades específicas de un agente tópico para ser utilizados en el transcurso de 1 semana o mes para garantizar el uso adecuado de los corticosteroides tópicos, TCI, y / o hidratantes.
Se debe pedir a los pacientes / cuidadores que lleven los envases usados o a medio usar al consultorio durante su próxima visita ya que puede ser útil en la evaluación de la adherencia (aunque siempre debe considerarse la posibilidad de desecho intencional o "dumping" del medicamento). A pesar de la instrucción adecuada, algunos pacientes / cuidadores pueden todavía no aplicar cantidades adecuadas de corticosteroides tópicos por temor a los efectos secundarios (es decir, "fobia a los esteroides").
Es necesario hacer conscientes a los pacientes / cuidadores de los signos de atrofia de la piel (por ejemplo, una mayor transparencia y brillo de la piel; estrías) y explicar que los efectos secundarios cutáneos leves son reversibles con el tiempo (pero las estrías lo son) pueden aliviar algunos de estos temores y aumentar la adherencia.
Los planes escritos y la educación del paciente / cuidador tiene el potencial de mejorar la adherencia al tratamiento, lo que es un determinante importante del éxito del tratamiento. Hay una serie de estrategias adicionales que los pediatras y los médicos de cabecera pueden utilizar para mejorar la adherencia entre sus pacientes, incluyendo a los pacientes/cuidadores en discusiones atractivas acerca de medicamentos / experiencias anteriores, sugiriendo el apoyo de grupos tales como la Asociación Nacional de Eczema (NEA;
http://nationaleczema.org/), para hacer frente a los efectos secundarios de forma proactiva, el refuerzo positivo, las visitas frecuentes de seguimiento, el acceso a las arreglaron cuidar el cumplimiento y la atención programas de manejo, y, en el la mayoría de los pacientes no cumplen las normas, aplicando medicamentos en el consultorio.
Los stikers gráficos pueden ser una herramienta particularmente útil para mejorar la adherencia entre los pacientes pediátricos.46 Muchos pacientes / cuidadores tal vez deseen examinar terapias complementarias y alternativas; éstas deben ser revisados con apertura mental, aunque en este tiempo no hay datos clínicos que apoyen la consideración de su uso.13
La derivación a un
psicólogo infantil es apropiada en los casos en que se necesita apoyo conductual del paciente y educación de los cuidadores. El NEA es un recurso valioso para el paciente / cuidador y el apoyo educativo. Existen folletos educativos disponibles para su distribución por proveedores de salud. En cuanto a los productos para el cuidado de la piel, NEA mantiene una lista los que han cumplido con los criterios de aceptación del Sello NEA para sensibilidad, seguridad y toxicidad, así como ingredientes, contenido y formulación.
Además, los médicos pueden encontrar útil formar grupos cooperativos de profesionales de la salud dentro de su práctica o zona local zona para facilitar la coordinación de la atención, intercambio de información y puesta en común de recursos.
Los pacientes / cuidadores, así como los pediatras y otros médicos de cabecera pueden encontrar recursos útiles en los siguientes sitios web:
• NEA: http://nationaleczema.org
• Información de DA de Asma y Allergy Foundation of America: http://www.aafa.org/display.cfm?id=9ysub=23&cont=325
• Centro de Eczema en Rady Hospital de Niños de San Diego: http://eczemacenter.org
• Centro Multidisciplinario de Eczema Noroeste:
http: //eczema.nm.org
• Programa Nacional Judío de Salud de Dermatitis Atópica Pediátricahttp://www.nationaljewish.org/programas/pediátrico/atopicdermatitis
• La información de DA desde la AAD: http://www.aad.org/dermatologya--az/enfermedades-y-tratamientos/a---d/atópicadermatitis
• La información de AD del Instituto Nacional de Artritis y Enfermedades Musculoesqueléticas y de la Piel: http: // www.niams.nih.gov/Health_Info/Dermatitisatópica
Conclusiones
Los pediatras y otros médicos de cabecera juegan un papel central en el manejo de la DA, ya sea por derivación de pacientes con DA moderada a severa para atención especializada, proporcionando atención de mantenimiento después de la evaluación por especialistas, o el manejo de los pacientes con DA leve o más episódica.
El modelo de tratamiento propuesto en este artículo está diseñado específicamente para su uso por los pediatras y otros médicos de cabecera e incluye medidas básicas de manejo (cuidado de la piel, medidas antisépticas, y la evitación de la activación) para ser utilizado independientemente de la gravedad de la DA, el tratamiento agudo de los brotes con corticosteroides tópicos de baja o media potencia, dependiendo de la severidad del brote y el tratamiento de mantenimiento con TCI y / o corticosteroides tópicos para los pacientes con enfermedad moderada a severa.
Porque el curso de la DA varía de paciente al paciente, es crítico para diseñar planes de tratamiento basados en los pacientes las y preferencias individuales de los cuidadores y necesidades, incluyendo la edad del paciente, el estilo de vida de la familia, la preferencia por formulación tópica de tratamiento, y el patrón de lesiones y brotes. La educación de pacientes y cuidadores debería incluir un plan de tratamiento por escrito e instrucción sobre la evitación de disparo y aplicación del tratamiento tópico en forma correcta.
Los planes de tratamiento deben ser continuamente optimizados y refinado durante el seguimiento regular.
Comentario:
La DA afecta a un gran número de pacientes, generando preocupación y morbilidad. Constituye un motivo frecuente de consulta en la práctica pediátrica.
La mayoría de los pacientes presenta enfermedad leve o moderada o con evolución por brotes y podría ser perfectamente tratada y seguida por el pediatra o médico de cabecera. Sin embargo, la mayoría de las veces estos niños son derivados a dermatólogos o inmunólogos para la confirmación diagnóstica y manejo. Esto podría deberse a que no hay suficiente difusión de guías de tratamiento dirigidas a médicos pediatras o generalistas.
El presente trabajo evaluó las guías disponibles, consensuando los criterios, recomendaciones de tratamiento, accesibilidad y aplicabilidad destinadas a médicos no especialistas, simplificando el modelo de tratamiento basado en la severidad de la DA, con evidencia clínica, producto de una mesa redonda multidisciplinaria. Es importante destacar que tanto el diagnóstico como el manejo de cada paciente es una situación única y diferente y es necesario individualizar los planes de tratamiento para cada uno, ajustándose a las sugerencias de las guías.
Resumen y comentario objetivo: Dra. María José Chiolo